Η υλοποίηση μιας κλινικής μελέτης είναι μια πολύπλοκη διαδικασία, η οποία απαιτεί και προϋποθέτει τη συμμετοχή πολλών μερών. Είναι σημαντικό, κάθε ένα από τα εμπλεκόμενα μέρη να έχει κατανοήσει τον ρόλο του σε αυτή τη διαδικασία.
Η επιλογή των χωρών για τη διεξαγωγή μιας κλινικής μελέτης στηρίζεται σε μια σειρά κριτηρίων με τα σημαντικότερα να είναι η ταχύτητα των διαδικασιών, η ύπαρξη ερευνητικών κέντρων με υψηλά ποσοτικά και ποιοτικά standards και γενικότερα η ύπαρξη ενός ευνοϊκού/φιλικού περιβάλλοντος για την κλινική έρευνα. Η μείωση της γραφειοκρατίας και η απλούστευση των διαδικασιών στα Νοσοκομεία και τους Φορείς Οικονομικής διαχείρισης μέσω ενός κατάλληλου θεσμικού πλαισίου είναι η πλέον βασική προϋπόθεση.
Η αξιοποίηση της ψηφιακής τεχνολογίας στην κατάθεση και υπογραφή των απαραίτητων εγγράφων θα συνεισφέρει σημαντική στην επιτάχυνση των διαδικασιών.
Η ίδρυση αυτοτελών τμημάτων κλινικών μελετών (Γραφεία Κλινικών Μελετών) στα Νοσοκομεία θα συνεισφέρει ουσιαστικά στον συντονισμό και την ταχύτερη διαχείριση των θεμάτων των κλινικών μελετών. Οι αποφάσεις των Διοικήσεων για την ίδρυση αυτών των τμημάτων στα Νοσοκομεία που πληρούν τις προϋποθέσεις είναι το επόμενο βήμα, το οποίο και είναι επιτακτικό να γίνει το συντομότερο δυνατό.
Η δημιουργία θέσης/ρόλου στο Υπουργείο Υγείας με αποκλειστική ευθύνη τις κλινικές μελέτες θα βοηθούσε σημαντικά στη συλλογή και επίλυση των προβλημάτων, αλλά και στην παρακολούθηση και τον έλεγχο των ποικίλων ζητημάτων που προκύπτουν καθημερινά. Η ανταγωνιστικότητα της χώρας μας στο πεδίο των κλινικών μελετών σχετίζεται σε μεγάλο βαθμό με τον ενεργό ρόλο του υπουργείου Υγείας.
Οι Φορείς Οικονομικής Διαχείρισης (ΕΛΚΕ/ΕΛΚΕΑ) διασφαλίζουν τη διαφάνεια και την ορθότητα στην οικονομική διαχείριση των κλινικών ερευνητικών προγραμμάτων. Για την αποφυγή της γραφειοκρατίας και των αδικαιολόγητων καθυστερήσεων, όπως για παράδειγμα στην υπογραφή των συμβάσεων, είναι απαραίτητο να υπάρξουν ενιαίες Πρότυπες Διαδικασίες (SOPs) με εφαρμογή σε όλους τους Φορείς και σε όλη την Επικράτεια.
Οι τοπικές Αρμόδιες Αρχές, για την Ελλάδα ο Εθνικός Οργανισμός Φαρμάκων (ΕΟΦ) και η Εθνική Επιτροπή Δεοντολογίας για τις Κλινικές Μελέτες (ΕΕΔ), επιτελούν καθοριστικό ρόλο, με τη γενική εποπτεία και την ευθύνη της δημιουργίας και της εφαρμογής του Κανονιστικού πλαισίου για τη διεξαγωγή της κλινικής έρευνας στη χώρα μας. Για να μπορούν οι Αρχές να ανταποκριθούν στις διαρκώς αυξανόμενες απαιτήσεις είναι απαραίτητη η διαχρονικά σταθερή στελέχωσή τους με επαρκή αριθμό κατάλληλα εκπαιδευμένων ατόμων, ζήτημα, το οποίο, στην παρούσα φάση, απαιτεί άμεση λύση. Είναι επίσης σημαντικό να υπάρξει η δυνατότητα καταγραφής/μέτρησης της δραστηριότητας της κλινικής έρευνας (αριθμός κλινικών μελετών, αριθμός ασθενών, οικονομικός απολογισμός, κλπ.) σε ετήσια βάση και εθνικό επίπεδο, στοιχεία, τα οποία σήμερα δεν είναι διαθέσιμα.
Η θεσμοθέτηση κατάλληλων για την κλινική έρευνα οικονομικών κινήτρων, που σήμερα δεν είναι επαρκή, θα συνεισέφερε σημαντικά.
Σύμφωνα με πρόσφατη έκθεση, η δραστηριότητα της Ευρώπης στις κλινικές μελέτες που χρηματοδοτούνται από φαρμακευτικές εταιρείες έχει υποχωρήσει σημαντικά. Η επιτάχυνση και η απλούστευση στις διαδικασίες θα αποτελέσουν τους κρίσιμους παράγοντες για την επιλογή μιας ευρωπαϊκής χώρας.
Η ευκαιρία υπάρχει και η Ελλάδα έχει τη δυνατότητα να διεκδικήσει δυναμικά τη συμμετοχή της στην κλινική έρευνα σε παγκόσμια κλίμακα.
Ειδήσεις υγείας σήμερα
Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή
Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού
Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης

 ΕΜΑ - Ευρωπαϊκό το μητρώο για τις κλινικές μελέτες που υιοθέτησε ο ΠΟΥ
ΕΜΑ - Ευρωπαϊκό το μητρώο για τις κλινικές μελέτες που υιοθέτησε ο ΠΟΥ 21μελής ομάδα εργασίας για τις κλινικές μελέτες - Συντονίστρια η Λ. Βιλδιρίδη - Ποιοι μετέχουν
21μελής ομάδα εργασίας για τις κλινικές μελέτες - Συντονίστρια η Λ. Βιλδιρίδη - Ποιοι μετέχουν Οι 10 κορυφαίες ευρωπαϊκές χώρες σε κλινικές δοκιμές το 2025
Οι 10 κορυφαίες ευρωπαϊκές χώρες σε κλινικές δοκιμές το 2025 Γεωργιάδης: Πόσο αυξήθηκαν οι κλινικές μελέτες το 2024 και τι αναμένεται φέτος
Γεωργιάδης: Πόσο αυξήθηκαν οι κλινικές μελέτες το 2024 και τι αναμένεται φέτος "Μαγικό μανιτάρι" εναντίον κατάθλιψης: Το ΑΠΘ σε πρωτοποριακή διεθνή κλινική μελέτη
"Μαγικό μανιτάρι" εναντίον κατάθλιψης: Το ΑΠΘ σε πρωτοποριακή διεθνή κλινική μελέτη Sanofi Ελλάδας: Εκδήλωση για την επένδυση στις κλινικές μελέτες παρουσία του Υπουργού Υγείας και της Πρέσβειρος της Γαλλίας
Sanofi Ελλάδας: Εκδήλωση για την επένδυση στις κλινικές μελέτες παρουσία του Υπουργού Υγείας και της Πρέσβειρος της Γαλλίας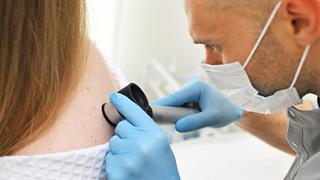 Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή
Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή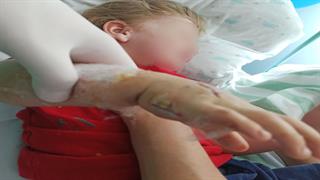 Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού
Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης
Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης Δράμα: Η μεγαλύτερη προκήρυξη θέσεων ιστορικά για το νοσοκομείο
Δράμα: Η μεγαλύτερη προκήρυξη θέσεων ιστορικά για το νοσοκομείο Η τροφή ως φάρμακο - Δεκάλογος διατροφικών αλλαγών για ένα υγιές ήπαρ
Η τροφή ως φάρμακο - Δεκάλογος διατροφικών αλλαγών για ένα υγιές ήπαρ 'Ερχεται ευρωπαϊκό πλαίσιο για την κοιλιοκάκη
'Ερχεται ευρωπαϊκό πλαίσιο για την κοιλιοκάκη Συστάθηκε η Ένωση Διαγνωστικών Εργαστηρίων Μοριακής Βιολογίας
Συστάθηκε η Ένωση Διαγνωστικών Εργαστηρίων Μοριακής Βιολογίας![Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη]](/media/articles/photos/thumb/132273-elfrydasippokr251280.jpg) Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη]
Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη]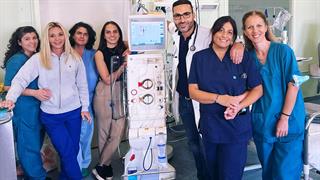 Χίος: Με δωρεές Χιωτών εκσυγχρονίζεται εκ βάθρων η Μονάδα Τεχνητού Νεφρού
Χίος: Με δωρεές Χιωτών εκσυγχρονίζεται εκ βάθρων η Μονάδα Τεχνητού Νεφρού "Αλεξάνδρα": Στις φλόγες ασθενής που υποβαλλόταν σε επέμβαση - Γεωργιάδης: Διατάχθηκε ΕΔΕ
"Αλεξάνδρα": Στις φλόγες ασθενής που υποβαλλόταν σε επέμβαση - Γεωργιάδης: Διατάχθηκε ΕΔΕ ΕΟΠΥΥ: Οδηγίες εγγραφής ασθενών στην πλατφόρμα κατ΄ οίκον αποστολής φαρμάκων υψηλού κόστους
ΕΟΠΥΥ: Οδηγίες εγγραφής ασθενών στην πλατφόρμα κατ΄ οίκον αποστολής φαρμάκων υψηλού κόστους![Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]](/media/articles/photos/thumb/132308-chicken.jpg) Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]
Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]