Καλύτερος έλεγχος στα διαπιστευτήρια που θα καταθέτουν οι εταιρείες (με έμφαση στο κλινικό όφελος-αποτελεσματικότητα) για την είσοδο των "προβαλλόμενων" καινοτόμων θεραπειών τους στην ελληνική αγορά, σωστότερη διαχείριση των θεραπειών με βάση τις πραγματικές ανάγκες, αλλά και ταχύτερη είσοδο στη χώρα θα είναι το τρίπτυχο της λειτουργίας του νέου Ταμείου για τις Καινοτόμες θεραπείες, το οποίο οργανωτικά θα στηθεί φέτος (προς τα τέλη του 2024) και θα ενεργοποιηθεί στις αρχές του 2025.
Τι μάθαμε για αυτό;
1) Αν και υπήρχε κάποια σύγχυση ως προς την χρηματοδότησή του νέου Ταμείου, η τελευταία πληροφόρηση που έχουμε είναι ότι έχουν ξεκινήσει συζητήσεις με το Υπουργείο Οικονομικών για την εξεύρεση κονδυλίων στήριξης του Ταμείου.
2) Θα αφορά αποκλειστικά τις γονιδιακές και κυτταρικές θεραπείες καθώς και τα ορφανά φάρμακα για σπάνιες παθήσεις.
Μολονότι, λένε πληροφορίες, υπήρχε πίεση από τις εταιρείες που διαχειρίζονται γονιδιακές και κυτταρικές θεραπείες το εν λόγω Ταμείο να αφορά μόνο αυτές, τελικά επικράτησε η άποψη του Υπουργείου Υγείας να περιλαμβάνονται και τα ορφανά φάρμακα. Η δαπάνη ειδικά για τα ορφανά φάρμακα, τουλάχιστον σε πρώτη φάση, επί της συνολικής που θα έχει το Ταμείο θα είναι από 50 έως 80 εκατ. ευρώ.
Σύμφωνα με τα τελευταία διαθέσιμα στοιχεία, 82 ορφανά φάρμακα αποζημιώνονται από τον ΕΟΠΥΥ ενώ 74 ορφανά φάρμακα διανέμονται μέσω ΙΦΕΤ (μέσω έκτακτης εισαγωγής). Από τα 267 εκατ. ευρώ περίπου που είναι ο προϋπολογισμός του ΙΦΕΤ, 92,8 εκατ. ευρώ αποτελούν τη δαπάνη για σπάνιες παθήσεις (ποσοστό 34,82%).
Οσον αφορά τη δαπάνη ορφανών φαρμάκων από τον ΕΟΠΥΥ, ήταν 3,6% το 2020, ενώ το 2023 έφθασε στο 5.7%. Εξαιρούνται φυσικά τα νοσοκομειακά φάρμακα, όπου εκεί έχουμε πολύ ακριβές θεραπείες.
3) Ο προϋπολογισμός του θα είναι από 200 ευρώ μέχρι και 300 ευρώ. Ο προϋπολογισμός αυτός θα αφορά κάποιες καινούργιες θεραπείες που θα έρθουν το 2025, ενώ θα συμπεριληφθούν και κάποιες θεραπείες που σήμερα διαχειρίζεται ο ΙΦΕΤ. Αρα και από εκεί θα προκύψει ένα επιπλέον κονδύλι για το νέο Ταμείο.
4) Προτεραιότητα θα έχουν τα ορφανά φάρμακα που διαθέτουν τη σχετική πιστοποίηση από τον ΕΜΑ. Αρα φάρμακα που έχουν πιστοποίηση από τον FDA αλλά όχι από τον ΕΜΑ μπαίνουν σε δεύτερη μοίρα. Θυμίζουμε το πρόσφατο παράδειγμα σκευάσματος που αποσύρθηκε με υπουργική εντολή από τη χώρα και το οποίο είχε έγκριση ως ορφανό από τον FDA και όχι τον ΕΜΑ, ενώ αποδεδειγμένα δεν είχε κανένα κλινικό όφελος.
5) Τον πρώτο λόγο, εισαγωγής των θεραπειών στο νέο Ταμείο θα έχει μία μικτή επιτροπή με επιστήμονες από τον ΕΟΠΥΥ και τον ΕΟΦ.
Η δημιουργία του νέου Ταμείου δεν είναι ελληνική εφεύρεση, καθώς υπάρχουν αρκετές περιπτώσεις άλλων κρατών που έχουν δημιουργήσει μοντέλα χρηματοδότησης που βασίζονται σε δημόσιο-ιδιωτικές συνεργασίες, ειδικών δωρεών συνδεδεμένων με πωλήσεις και συμπράξεις που στοχεύουν στην απόκτηση συμπληρωματικών κεφαλαίων για τη στήριξη των καινοτόμων μεν πανάκριβων δε θεραπειών.
Για παράδειγμα, στη Σκωτία, η δημιουργία του Νέου Ταμείου Φαρμάκων που έχει συσταθεί από το 2013 διευκολύνει την πρόσβαση σε ορφανά φάρμακα, ενώ στη Σιγκαπούρη έχει συσταθεί ειδικό ταμείο για την υποστήριξη ατόμων με σπάνιες παθήσεις, συνδυάζοντας δωρεές και κυβερνητική αντιστοίχιση συνεισφορών. Το Υπουργείο Υγείας (MOH) και το SingHealth Fund έχουν ιδρύσει από κοινού το Ταμείο Σπάνιων Ασθενειών (RDF), ένα φιλανθρωπικό ταμείο που συνδυάζει κοινοτικές δωρεές με αντίστοιχη κρατική συνεισφορά για την υποστήριξη των πολιτών της Σιγκαπούρης με συγκεκριμένες σπάνιες ασθένειες που χρειάζονται θεραπεία με υψηλό κόστος φάρμακα.
Πάντως, σε όλη την Ευρώπη πλανάται το ερώτημα πώς θα μπορέσει να τετραγωνίσει τον κύκλο, κοινώς να αποζημιώσει και να εκμεταλλευτεί πλήρως τις νέες θεραπείες που αν και -κάποιες- εμφανίζουν επιπρόσθετο κλινικό όφελος είναι πανάκριβες.
Στο πλαίσιο αυτό έχει αποφασιστεί ότι από το 2025, όλες οι κυτταρικές και γονιδιακές θεραπείες θα υποβάλλονται σε μια ενιαία αξιολόγηση της ΕΕ για την αξία που προσθέτουν στους ασθενείς και τα συστήματα υγείας, γεγονός που αναμένεται να τερματίσει την ανάγκη για 27 διπλές αναθεωρήσεις.
Θυμίζουμε ότι από επτά από τις 25 κυτταρικές και γονιδιακές θεραπείες που έχουν εγκριθεί στην Ευρώπη έχουν ήδη αποσυρθεί από τις τις αγορές της ΕΕ, λόγω των αδυναμιών αποζημίωσής τους. Ετσι από το 2018, η αγορά κυτταρικής και γονιδιακής θεραπείας στην ΕΕ έχει αυξηθεί μόλις κατά 11 τοις εκατό, σε σύγκριση με 43 τοις εκατό στις ΗΠΑ και 531 τοις εκατό στην Κίνα.
Ειδήσεις υγείας σήμερα
Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή
Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού
Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης

 Πρώτη παγκόσμια κλινική δοκιμή για in vivo γονιδιακή θεραπεία
Πρώτη παγκόσμια κλινική δοκιμή για in vivo γονιδιακή θεραπεία Πρώτη τοπική γονιδιακή θεραπεία για τη πομφολυγώδη επιδερμόλυση
Πρώτη τοπική γονιδιακή θεραπεία για τη πομφολυγώδη επιδερμόλυση Γονιδιακή θεραπεία για μικρά παιδιά με δυστροφία αμφιβληστροειδούς
Γονιδιακή θεραπεία για μικρά παιδιά με δυστροφία αμφιβληστροειδούς Κυτταρικές και γονιδιακές θεραπείες: Μϊα "νέα Ιατρική", προκλήσεις και προβληματισμοί
Κυτταρικές και γονιδιακές θεραπείες: Μϊα "νέα Ιατρική", προκλήσεις και προβληματισμοί Γονιδιακή θεραπεία αναστρέφει την καρδιακή ανεπάρκεια σε χοίρους
Γονιδιακή θεραπεία αναστρέφει την καρδιακή ανεπάρκεια σε χοίρους  Γονιδιακή υπογραφή RNA καθοδηγεί τη χημειοθεραπεία στον τριπλά αρνητικό καρκίνο του μαστού
Γονιδιακή υπογραφή RNA καθοδηγεί τη χημειοθεραπεία στον τριπλά αρνητικό καρκίνο του μαστού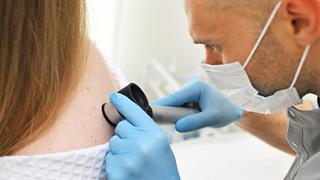 Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή
Ποια αλλαγή στο δέρμα προκαλείται από την κλιματική αλλαγή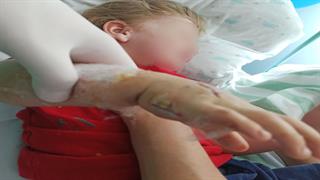 Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού
Δάγκωμα οχιάς: Γιατί είναι απαραίτητη η εμπλοκή και του ορθοπαιδικού Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης
Διατροφή που μπορεί να βοηθήσει με την εφίδρωση της εμμηνόπαυσης Δράμα: Η μεγαλύτερη προκήρυξη θέσεων ιστορικά για το νοσοκομείο
Δράμα: Η μεγαλύτερη προκήρυξη θέσεων ιστορικά για το νοσοκομείο Η τροφή ως φάρμακο - Δεκάλογος διατροφικών αλλαγών για ένα υγιές ήπαρ
Η τροφή ως φάρμακο - Δεκάλογος διατροφικών αλλαγών για ένα υγιές ήπαρ 'Ερχεται ευρωπαϊκό πλαίσιο για την κοιλιοκάκη
'Ερχεται ευρωπαϊκό πλαίσιο για την κοιλιοκάκη Συστάθηκε η Ένωση Διαγνωστικών Εργαστηρίων Μοριακής Βιολογίας
Συστάθηκε η Ένωση Διαγνωστικών Εργαστηρίων Μοριακής Βιολογίας![Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη]](/media/articles/photos/thumb/132273-elfrydasippokr251280.jpg) Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη]
Καθαριστής αέρα σε θάλαμο CoViD-19 μείωσε κατά 98,1% το ιικό φορτίο [ελληνική μελέτη] Χίος: Με δωρεές Χιωτών εκσυγχρονίζεται εκ βάθρων η Μονάδα Τεχνητού Νεφρού
Χίος: Με δωρεές Χιωτών εκσυγχρονίζεται εκ βάθρων η Μονάδα Τεχνητού Νεφρού "Αλεξάνδρα": Στις φλόγες ασθενής που υποβαλλόταν σε επέμβαση - Γεωργιάδης: Διατάχθηκε ΕΔΕ
"Αλεξάνδρα": Στις φλόγες ασθενής που υποβαλλόταν σε επέμβαση - Γεωργιάδης: Διατάχθηκε ΕΔΕ ΕΟΠΥΥ: Οδηγίες εγγραφής ασθενών στην πλατφόρμα κατ΄ οίκον αποστολής φαρμάκων υψηλού κόστους
ΕΟΠΥΥ: Οδηγίες εγγραφής ασθενών στην πλατφόρμα κατ΄ οίκον αποστολής φαρμάκων υψηλού κόστους![Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]](/media/articles/photos/thumb/132308-chicken.jpg) Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]
Η τακτική κατανάλωση κοτόπουλου αυξάνει τον κίνδυνο θανάτου από καρκίνο του πεπτικού [μελέτη]