«Το 10 έως 30 τοις εκατό των ασθενών με καρκίνο του πνεύμονα παγκοσμίως, έχουν όγκους που είναι θετικοί σε ορισμένες μεταλλάξεις του EGFR», είπε ο Hal Barron, M.D., Ιατρικός Διευθυντής και Επικεφαλής του τμήματος Ανάπτυξης Προϊόντων της Roche. «Οι άνθρωποι με αυτό τον τύπο καρκίνου του πνεύμονα έχουν πλέον την επιλογή να λάβουν ένα εξατομικευμένο φάρμακο ως θεραπεία πρώτης γραμμής, το οποίο θα τους βοηθήσει να επιτύχουν μεγαλύτερη επιβίωση χωρίς εξέλιξη της νόσου τους».
«Οι γιατροί και οι ασθενείς βασίζονται ολοένα και περισσότερο σε διαγνωστικά μέσα που τους βοηθούν στη λήψη εξατομικευμένων θεραπευτικών αποφάσεων. Η έγκριση του cobas EGFR Mutation Test υπογραμμίζει τη σημασία που έχει μία ευαίσθητη δοκιμασία ακριβείας που μπορεί να πραγματοποιηθεί έγκαιρα, στη λήψη κρίσιμων θεραπευτικών αποφάσεων», είπε ο Paul Brown, επικεφαλής του τμήματος Μοριακών Διαγνωστικών της Roche. «Στη Roche, έχουμε αναλάβει μία βαθιά δέσμευση για την παροχή εξατομικευμένων επιλογών υγειονομικής περίθαλψης και σήμερα αναπτύσσουμε συνοδευτικές διαγνωστικές εφαρμογές για περισσότερα από τα μισά φάρμακα που βρίσκονται σε στάδιο ανάπτυξης».
Ειδήσεις υγείας σήμερα
Πώς φροντίζω κάθε τύπο δέρματος
Καρδιακή προσβολή: Οι β-αναστολείς συνδέονται με κατάθλιψη στη μετεγχειρητική φροντίδα
Δράμα: Κανένα ενδιαφέρον για 5 θέσεις παθολόγων, παρά το επίδομα άγονου

 Αστυνομικός ενημερώθηκε ότι είχε καρκίνο με καθυστέρηση ενός χρόνου
Αστυνομικός ενημερώθηκε ότι είχε καρκίνο με καθυστέρηση ενός χρόνου Bιοδείκτες
Bιοδείκτες Επίπτωση καρκίνου σε ασθενείς και εργοδότες - Το κόστος της υγειονομικής περίθαλψης
Επίπτωση καρκίνου σε ασθενείς και εργοδότες - Το κόστος της υγειονομικής περίθαλψης Το σελήνιο "κλειδί" στη μάχη κατά του παιδιατρικού καρκίνου
Το σελήνιο "κλειδί" στη μάχη κατά του παιδιατρικού καρκίνου Θεσσαλονίκη: Εγκαινιάστηκε το Διεθνές Ογκολογικό Κέντρο του Ομίλου Ιατρικού Αθηνών
Θεσσαλονίκη: Εγκαινιάστηκε το Διεθνές Ογκολογικό Κέντρο του Ομίλου Ιατρικού Αθηνών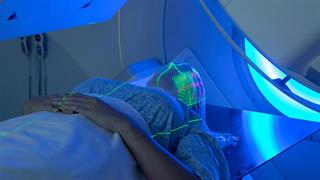 Ακτινοθεραπεία: Το εξελιγμένο όπλο στην καταπολέμηση του καρκίνου
Ακτινοθεραπεία: Το εξελιγμένο όπλο στην καταπολέμηση του καρκίνου Πώς φροντίζω κάθε τύπο δέρματος
Πώς φροντίζω κάθε τύπο δέρματος Καρδιακή προσβολή: Οι β-αναστολείς συνδέονται με κατάθλιψη στη μετεγχειρητική φροντίδα
Καρδιακή προσβολή: Οι β-αναστολείς συνδέονται με κατάθλιψη στη μετεγχειρητική φροντίδα Δράμα: Κανένα ενδιαφέρον για 5 θέσεις παθολόγων, παρά το επίδομα άγονου
Δράμα: Κανένα ενδιαφέρον για 5 θέσεις παθολόγων, παρά το επίδομα άγονου Περιεμμηνόπαυση: Ερωτήσεις που πρέπει να κάνετε στον γυναικολόγο σας
Περιεμμηνόπαυση: Ερωτήσεις που πρέπει να κάνετε στον γυναικολόγο σας 30 δραστικές ουσίες εκτός θετικού καταλόγου
30 δραστικές ουσίες εκτός θετικού καταλόγου Πέθανε ο ψυχίατρος Δημήτρης Σούρας - Η ανάρτηση στον προσωπικό του λογαριασμό
Πέθανε ο ψυχίατρος Δημήτρης Σούρας - Η ανάρτηση στον προσωπικό του λογαριασμό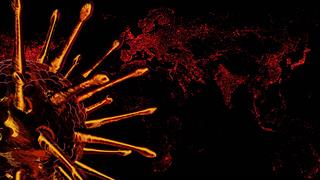 Μελέτη συνδέει τη λοίμωξη COVID-19 με ύφεση καρκινικών όγκων
Μελέτη συνδέει τη λοίμωξη COVID-19 με ύφεση καρκινικών όγκων Tέλος η ταινία γνησιότητας στα φάρμακα
Tέλος η ταινία γνησιότητας στα φάρμακα Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους
Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους Self test για πρόληψη καρκίνου παχέος εντέρου: Τι σημαίνει το θετικό ή αρνητικό αποτέλεσμα
Self test για πρόληψη καρκίνου παχέος εντέρου: Τι σημαίνει το θετικό ή αρνητικό αποτέλεσμα ‘Eχετε αυξημένη ή χαμηλή Β12; Τι πρέπει να ξέρετε
‘Eχετε αυξημένη ή χαμηλή Β12; Τι πρέπει να ξέρετε Νέα εξαγορά από την οικογένεια Σκλαβενίτη
Νέα εξαγορά από την οικογένεια Σκλαβενίτη